病灶消除,GC101 TIL疗法使KRAS突变肺癌患者持续获益
近日,君赛生物临床试验中,一例KRAS突变阳性肺癌受试者经GC101 TIL治疗18周后,疗效评估靶病灶达到完全缓解(CR),非靶病灶正逐渐消退,为KRAS突变阳性肺癌患者带来希望。
该受试者是KRAS G12D突变的肺腺癌ⅣB期患者,自2022年4月出现左胸疼痛,确诊后先后接受免疫与化疗的联合治疗,以及免疫、抗血管生成抑制剂与化疗的联合治疗,都因疾病进展或不耐受停药。在现有治疗手段无效时,患者参加了君赛生物GC101 TIL细胞注射液注册临床试验。
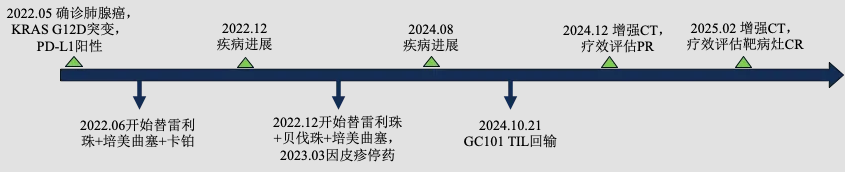
患者接受治疗过程
GC101 TIL细胞疗法依托君赛生物DeepTILTM细胞扩增平台研发而成,无需高浓度IL-2和滋养细胞即可培养出足够数量的高活性TIL细胞,且对IL-2无依赖性。临床应用中,GC101无需高强度清淋化疗和IL-2给药,有效解决了常规TIL依赖大剂量化疗清淋预处理,大剂量IL-2注射的临床痛点。
TIL治疗过程,受试者除预处理过程短暂血液学毒性外无其他不良反应。回输第6周肿瘤缩小45%,肿瘤标志物恢复正常,癌痛减轻、颈部淋巴结消失;第12周靶病灶CR,18周时CR仍维持。
GC101 TIL展现出卓越疗效,仅需单次给药,便可持续发挥对肿瘤的杀伤作用。接受GC101 TIL治疗后,该受试者身体状况持续向好。得益于TIL疗法的长效性,受试者无需频繁返院接受额外治疗,定期回院进行随访也无需家属协助。在日常生活中,受试者完全能够自理,顺利回归正常家庭生活,这充分彰显了GC101 TIL在改善患者生活质量、助力患者回归正常生活方面的显著优势。
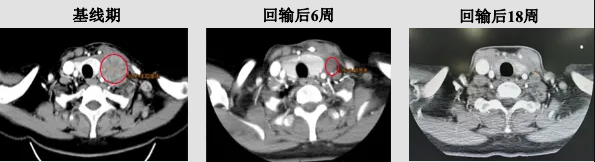
患者接受TIL治疗前和治疗后6周、18周增强CT扫描结果(左侧颈部淋巴结)
关于GC101
GC101是君赛生物研发进度最快的TIL疗法管线,也是全球首款无需高强度清淋化疗、无需IL-2给药的天然TIL疗法。
GC101依托君赛生物自主开发、全球领先的DeepTILTM细胞富集扩增平台开发而成,目前已进入关键II期临床(MIZAR-003),正在全国20个省(直辖市、自治区)的24个中心进行患者招募。(临床招募|君赛生物GC101 TIL治疗黑色素瘤的关键II期临床试验进行中)
已有临床数据显示,GC101针对多种类型晚期实体肿瘤的客观缓解率(ORR)超35%,已有多例患者肿瘤被完全清除,获得完全缓解(CR)疗效,其中无瘤生存最久时间已超3年。
关于DeepTILTM细胞富集扩增平台
DeepTILTM细胞富集扩增平台(Dual-free (ex vivo feeder cell & in vivo IL-2 free) expansion with optimized potency)实现无需高浓度IL-2和滋养细胞即可培养出足够数量的高活性TIL细胞,且不依赖于IL-2。在临床应用中,GC101无需高强度清淋化疗且无需IL-2给药,就能展现出卓越的疗效。
DeepTILTM细胞富集扩增平台赋予TIL细胞深入肿瘤内部发挥高效杀伤的能力,确保给患者带来深入且持久的疗效。
关于MIZAR-005临床试验
MIZAR-005是一项评价自体天然肿瘤浸润淋巴细胞注射液(GC101 TIL)治疗晚期非小细胞肺癌患者安全性和有效性的开放标签、单臂、Ⅰb期临床试验。
本临床试验项目在上海市胸科医院、安徽省胸科医院、湖南省肿瘤医院等医疗机构进行受试者招募及筛选,招募主要标准如下。
主要入组标准:
1、18-70岁,男女不限;
2、确诊的不可切除的晚期非小细胞肺癌患者;
3、经过靶向(如有上市药物)及含铂双药化疗治疗后失败;
4、至少2个病灶,身体可支持微创手术取材;
5、ECOG评分0-1分;
6、有足够的血液学和终末器官功能。
主要排除标准:
1、有严重基础性疾病;
2、有重大传染性疾病;
3、肺纤维化、间质性肺病(包括病史)、急性肺病;
4、脑转移且伴有临床症状或病灶大小不稳定。
联系方式:
临床邮箱:clinicaltrials@juncell.com
联系电话:021-69990503
杨老师:18019732895(同微信)
张老师:18001759113(同微信)
